ประเภท: บทความเด่น » ช่างไฟฟ้าสามเณร
จำนวนการดู: 36288
ความคิดเห็นเกี่ยวกับบทความ: 1
แหล่งเคมีปัจจุบัน: ลักษณะสำคัญ
 เป็นเวลากว่าสองศตวรรษที่มนุษย์ใช้พลังงานจากปฏิกิริยาเคมีระหว่างสารต่าง ๆ เพื่อผลิตกระแสตรง
เป็นเวลากว่าสองศตวรรษที่มนุษย์ใช้พลังงานจากปฏิกิริยาเคมีระหว่างสารต่าง ๆ เพื่อผลิตกระแสตรง
หลักการทำงาน
ปฏิกิริยารีดอกซ์ที่เกิดขึ้นระหว่างสารที่มีคุณสมบัติของตัวออกซิไดซ์และตัวรีดิวซ์นั้นจะมาพร้อมกับการปล่อยอิเล็คตรอนซึ่งเป็นการเคลื่อนที่ของกระแสไฟฟ้า อย่างไรก็ตามเพื่อที่จะใช้พลังงานจำเป็นต้องสร้างเงื่อนไขสำหรับการผ่านของอิเล็กตรอนผ่านวงจรภายนอกไม่เช่นนั้นความร้อนจะถูกปล่อยออกมาจากส่วนผสมที่เรียบง่ายของสารออกซิไดซ์และตัวรีดิวซ์
ดังนั้นแหล่งที่มาทางเคมีทั้งหมดจึงมีขั้วไฟฟ้าสองอัน:
-
ขั้วบวกที่เกิดออกซิเดชัน
-
แคโทดดำเนินการคืนค่าของสาร
อิเล็กโทรดที่ระยะไกลจะถูกวางไว้ในภาชนะที่มีอิเล็กโทรไลต์ซึ่งเป็นสารที่นำกระแสไฟฟ้าเนื่องจากกระบวนการแยกตัวของตัวกลางออกเป็นไอออน
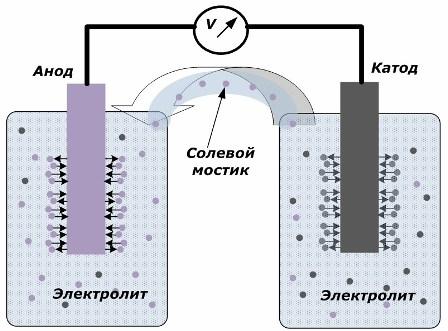
หลักการเปลี่ยนพลังงานเคมีเป็นพลังงานไฟฟ้า
รูปแสดงให้เห็นว่าขั้วไฟฟ้านั้นวางอยู่ในภาชนะที่แยกจากกันซึ่งเชื่อมต่อกันด้วยสะพานเกลือซึ่งทำให้เกิดการเคลื่อนที่ของไอออนตามวงจรภายใน เมื่อมีการเปิดวงจรภายนอกและภายในสองกระบวนการเกิดขึ้นบนขั้วไฟฟ้า: การเปลี่ยนไอออนจากโลหะของขั้วไฟฟ้าไปยังอิเล็กโทรไลต์และการเปลี่ยนแปลงของไอออนจากอิเล็กโทรไลต์ไปยังผลึกคริสตัลของขั้วไฟฟ้า
อัตราการไหลของกระบวนการเหล่านี้เหมือนกันและศักย์ไฟฟ้าของสัญญาณตรงข้ามสะสมในแต่ละอิเล็กโทรด หากมีการเชื่อมต่อผ่านสะพานเกลือและมีการใช้โหลดวงจรไฟฟ้าจะเกิดขึ้น กระแสภายในถูกสร้างขึ้นโดยการเคลื่อนที่ของไอออนระหว่างอิเล็กโทรดผ่านอิเล็กโทรไลต์และสะพานเกลือ การเคลื่อนที่ของอิเล็กตรอนไปตามวงจรภายนอกในทิศทางจากขั้วบวกไปยังแคโทด
ปฏิกิริยารีดอกซ์เกือบทั้งหมดมาพร้อมกับการผลิตกระแสไฟฟ้า แต่มูลค่าของมันขึ้นอยู่กับปัจจัยหลายอย่างรวมถึงปริมาณและมวลของสารเคมีที่ใช้วัสดุที่ใช้ทำขั้วไฟฟ้าเช่นอิเล็กโทรไลต์ความเข้มข้นของไอออนการออกแบบ
มีการใช้กันอย่างแพร่หลายในปัจจุบันแหล่งเคมีปัจจุบัน:
-
สำหรับวัสดุของขั้วบวก (ตัวรีดิวซ์), สังกะสี (Zn), ตะกั่ว (Pb), แคดเมียม (Cd) และโลหะอื่น ๆ ;
-
สำหรับวัสดุแคโทด (ออกซิไดเซอร์) - ตะกั่วออกไซด์ PbO2, แมงกานีสออกไซด์ MnO2, นิกเกิลไฮดรอกไซด์ NiOOH และอื่น ๆ ;
-
อิเล็กโทรไลต์ขึ้นอยู่กับการแก้ปัญหาของกรดด่างหรือเกลือ
วิธีการจำแนกประเภท
ส่วนหนึ่งของแหล่งพลังงานเคมีสามารถนำกลับมาใช้ใหม่ได้ในขณะที่ส่วนอื่นไม่สามารถทำได้ หลักการนี้ใช้เป็นพื้นฐานสำหรับการจำแนกประเภทของพวกเขา
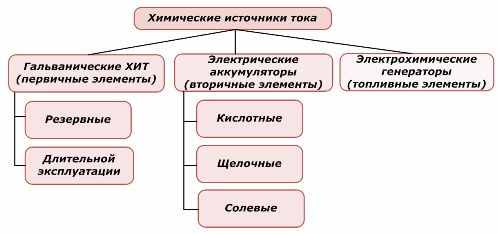
การจำแนกองค์ประกอบทางเคมี
แรงเคลื่อนไฟฟ้า เซลล์ไฟฟ้าขึ้นอยู่กับการออกแบบที่ระดับ 1.2 ÷ 1.5 โวลต์ เพื่อให้ได้ค่ามากจะรวมเข้ากับแบตเตอรี่เชื่อมต่อเป็นอนุกรม เมื่อเชื่อมต่อแบตเตอรี่แบบขนานกระแสและพลังงานจะเพิ่มขึ้น
เป็นที่ยอมรับกันโดยทั่วไปว่าแหล่งที่มาหลักทางเคมีในปัจจุบันไม่สนับสนุนการชาร์จใหม่แม้ว่าตำแหน่งนี้จะสามารถกำหนดสูตรได้แตกต่างกันมากขึ้น: การใช้งานนั้นไม่เป็นไปได้ทางเศรษฐกิจ
แหล่งกระแสเคมีหลักที่ซ้ำซ้อนจะถูกเก็บไว้ในสถานะที่แยกอิเล็กโทรไลต์ออกจากขั้วไฟฟ้า สิ่งนี้จะช่วยลดการเกิดปฏิกิริยารีดอกซ์และสร้างความมั่นใจในความพร้อมสำหรับการทดสอบเดินเครื่อง พวกเขาจะไม่ถูกนำมาใช้ซ้ำ อายุการเก็บรักษาของแหล่งพลังงานสำรองทางเคมีนั้น จำกัด อยู่ที่ 10-15 ปี
แบตเตอรี่สามารถชาร์จใหม่ได้โดยใช้พลังงานไฟฟ้าจากภายนอก เนื่องจากคุณสมบัตินี้พวกเขาจะเรียกว่าแหล่งที่มาปัจจุบันรอง พวกเขาสามารถทนต่อการปล่อยประจุได้หลายแสนรอบEMF ของแบตเตอรี่สามารถอยู่ในช่วง 1.0 ÷ 1.5 โวลต์ พวกเขารวมกันเป็นแบตเตอรี่
เครื่องกำเนิดไฟฟ้าทำหน้าที่เกี่ยวกับหลักการของเซลล์กัลวานิค แต่เพื่อทำปฏิกิริยาทางเคมีไฟฟ้าสารที่มาจากภายนอกและผลิตภัณฑ์ที่ปล่อยออกมาทั้งหมดจะถูกลบออกจากอิเล็กโทรไลต์ สิ่งนี้ช่วยให้คุณสามารถจัดระเบียบกระบวนการต่อเนื่อง
ลักษณะการทำงานที่สำคัญของแหล่งพลังงานเคมี
1. แรงดันไฟฟ้าข้ามขั้วเปิด
ขึ้นอยู่กับการออกแบบแหล่งเดียวสามารถสร้างความแตกต่างที่อาจเกิดขึ้นเท่านั้น สำหรับใช้ในอุปกรณ์ไฟฟ้าจะถูกรวมเข้ากับแบตเตอรี่
2. ความจุที่เฉพาะเจาะจง
ในบางช่วงเวลา (เป็นชั่วโมง) แหล่งเคมีหนึ่งแหล่งสามารถสร้างกระแสไฟฟ้าจำนวน จำกัด (เป็นแอมแปร์) ซึ่งมีสาเหตุมาจากหน่วยของน้ำหนักหรือปริมาตร
3. ความหนาแน่นพลังงาน
มันเป็นลักษณะความสามารถของหน่วยน้ำหนักหรือปริมาตรของแหล่งกำเนิดกระแสเคมีเพื่อสร้างพลังงานที่สร้างขึ้นโดยผลิตภัณฑ์ของแรงดันไฟฟ้าโดยความแรงของกระแส
4. ระยะเวลาการทำงาน
พารามิเตอร์นี้เรียกว่าวันหมดอายุ
5. มูลค่าของกระแสการปลดปล่อยตัวเอง
กระบวนการด้านปฏิกิริยาเคมีไฟฟ้าเหล่านี้จะนำไปสู่การบริโภคมวลที่ใช้งานขององค์ประกอบทำให้เกิดการกัดกร่อนและลดความสามารถเฉพาะ
6. ราคาสินค้า
ขึ้นอยู่กับการออกแบบวัสดุที่ใช้และปัจจัยอื่น ๆ
แหล่งที่มาทางเคมีที่ดีที่สุดคือแหล่งที่มีค่าสูงของพารามิเตอร์สี่ตัวแรกและการปลดปล่อยตัวเองและค่าใช้จ่ายต่ำ
หลักการชาร์จแบตเตอรี่
ในบรรดาแหล่งสารเคมีทุติยภูมิที่ได้รับความนิยมอย่างมาก ลิเธียมไอออนรุ่น ซึ่งได้กลายเป็นที่ใช้กันอย่างแพร่หลายเพื่อพลังงานอุปกรณ์อิเล็กทรอนิกส์ พวกเขาใช้ LiMO2 (M Co, Ni, Mn) เป็นวัสดุของขั้วบวกและกราไฟท์เป็นขั้วลบ
เมื่อประจุลิเธียมไอออนจากพลังงานภายนอกที่นำไปใช้จะถูกปล่อยออกมาจากโลหะแคโทดผ่านอิเล็กโทรไลต์และเจาะเข้าไปในช่องว่างระหว่างชั้นกราไฟท์สะสมอยู่ที่นั่น
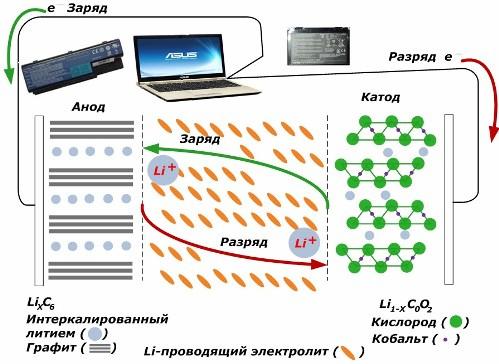
เมื่อพลังงาน ชาร์จ ไม่มีอยู่และโหลดเชื่อมต่อกับขั้วไฟฟ้าจากนั้นลิเธียมไอออนในอิเล็กโทรไลต์จะเคลื่อนที่ไปในทิศทางตรงกันข้าม
หากการชาร์จและการคายประจุไม่ได้ดำเนินการพลังงานในแบตเตอรี่จะไม่ถูกใช้ แต่จะถูกเก็บไว้ แต่ปริมาณจะถูก จำกัด ด้วยคุณสมบัติของวัสดุที่ใช้ ตัวอย่างเช่นในแบตเตอรี่ลิเธียมไอออนความจุไฟฟ้าเฉพาะคือ 130 ÷ 150 mAh / g มันถูก จำกัด โดยคุณสมบัติของวัสดุขั้วบวก สำหรับกราไฟท์ความจุจะสูงกว่าประมาณสองเท่า
นักวิทยาศาสตร์กำลังมองหาวิธีเพิ่มความจุของแบตเตอรี่กำลังค้นหาความเป็นไปได้ของการใช้ปฏิกิริยาทางเคมีระหว่างลิเธียมกับออกซิเจนในอากาศ เมื่อต้องการทำเช่นนี้การออกแบบได้รับการพัฒนาด้วยอากาศแคโทดที่ไม่สามารถใช้ได้ซึ่งใช้ในแบตเตอรี่แยกต่างหาก วิธีนี้สามารถเพิ่มความหนาแน่นพลังงานได้สูงสุด 10 เท่า
การดำเนินงานของแหล่งเคมีในปัจจุบันต้องมีความรู้ พื้นฐานของวิศวกรรมไฟฟ้าเคมีไฟฟ้าวัสดุศาสตร์และฟิสิกส์สถานะของแข็ง
ดูได้ที่ e.imadeself.com
:
