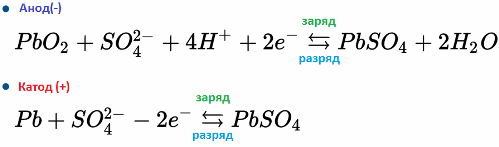Catégories: Comment ça marche, Électricien automobile
Nombre de fois vus: 16526
Commentaires sur l'article: 0
L'appareil et le principe de fonctionnement sur batterie
La batterie électrique s'appelle source de courant chimique réutilisable. Les processus chimiques à l'intérieur de la batterie, contrairement à ceux des piles galvaniques jetables, telles que les piles alcalines ou au sel, sont réversibles. Les cycles de charge-décharge, d'accumulation et de retour d'énergie électrique peuvent être répétés plusieurs fois.
Ainsi, le principe de fonctionnement de la batterie vous permet de l'utiliser cycliquement pour l'alimentation autonome d'une variété d'appareils, d'appareils portables, de véhicules, d'équipements médicaux, etc. dans des domaines complètement différents.

Parlant du mot "batterie", ils signifient soit la batterie elle-même, soit la cellule de la batterie. Plusieurs séries ou parallèles connectées les unes aux autres forment une batterie, ainsi que plusieurs batteries connectées.
La première batterie, c'est-à-dire une cellule galvanique réutilisable, est apparue, selon les chiffres officiels, en 1803. Il a été créé par le physicien et chimiste allemand Johann Wilhelm Ritter. Un ami d'Oersted, Ritter, n'étant pas scientifique, a étudié l'effet chimique de la lumière, a mené des expériences d'électrolyse, d'ailleurs, il appartient à la découverte de la partie ultraviolette du spectre électromagnétique.
En expérimentant avec une colonne voltaïque, Ritter a pris cinquante cercles de cuivre, des morceaux de tissu humide et a formé une colonne de cinquante de ces cercles et un tissu humide entre eux. En passant le courant de la colonne voltaïque à travers la structure, Ritter a découvert que son poteau était chargé et est devenu lui-même une source d'électricité. Ce fut la première batterie.
La réversibilité de la réaction chimique dans l'électrolyte et sur les électrodes de la batterie vous permet de restaurer l'efficacité de la batterie - chargez-la après décharge. Le courant pendant la charge passe à travers la batterie dans la direction opposée à la décharge.
Par exemple, une batterie plomb-acide fonctionne en raison des réactions électrochimiques du plomb et du dioxyde de plomb dans l'acide sulfurique. Les formules ci-dessous reflètent les réactions réversibles se produisant sur l'anode et sur la cathode: de gauche à droite - réaction pendant la décharge, de droite à gauche - charge.
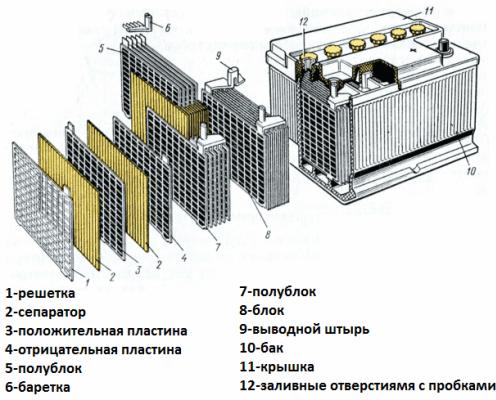
Considérez maintenant le dispositif de batterie comme un exemple de batterie de démarrage de voiture. Sa tension est de 12 volts. La batterie se compose de six cellules connectées en série, séparées par des partitions.
Dans ce cas, la connexion série signifie que la borne négative d'une cellule est connectée à la borne positive de la cellule suivante.
Chaque élément comprend une paire d'électrodes en treillis d'un alliage plomb-antimoine immergé dans un électrolyte, qui est une solution aqueuse à 38% d'acide sulfurique. Le séparateur poreux isole les électrodes les unes des autres, empêchant les courts-circuits entre elles, mais passe librement l'électrolyte à travers lui-même. C'est-à-dire que le liquide remplit à la fois les cellules des plaques de plomb et les pores des séparateurs.
Les plaques du même nom sont interconnectées par des cavaliers en plomb, ainsi que les boîtiers de plaques séparés par des cloisons, qui constituent des éléments individuels, et les bornes de la batterie sont également en plomb.
Les conclusions de la batterie de la voiture sont toujours légèrement différentes les unes des autres - la borne positive a un diamètre plus grand que la borne négative afin de ne pas faire d'erreur lors de la connexion.
Le boîtier de la batterie est fait d'un matériau diélectrique résistant aux environnements agressifs, aux températures extrêmes et aux vibrations. Aujourd'hui, les boîtiers de batterie de démarrage sont en polypropylène.
Le boîtier est un récipient hermétiquement scellé avec un couvercle, équipé de brides pour un montage durable.Dans les boîtiers des anciennes batteries, des bouchons étaient toujours prévus pour chacune des cellules galvaniques composant la batterie, afin que de l'eau distillée puisse être ajoutée si nécessaire. Les prises de batterie modernes sans entretien sur les boîtiers n'ont pas.
Autres articles sur les piles et leur utilisation:
Schémas de connexion de la batterie
Comment sont les batteries pour les centrales solaires
Comment les chargeurs de batterie sont-ils organisés et fonctionnent-ils?
Voir aussi sur e.imadeself.com
: