категории: Препоръчани статии » Интересни електрически новини
Брой преглеждания: 15067
Коментари към статията: 1
Литиево-йонни батерии
 Принципът на работа на всяка електрическа батерия е натрупването на електрическа енергия по време на химическата реакция, която възниква, когато зареждащият електрически ток протича през акумулатора, и генерирането на електрическа енергия, когато разрядният ток тече по време на обратната химическа реакция.
Принципът на работа на всяка електрическа батерия е натрупването на електрическа енергия по време на химическата реакция, която възниква, когато зареждащият електрически ток протича през акумулатора, и генерирането на електрическа енергия, когато разрядният ток тече по време на обратната химическа реакция.
Обратимостта на химическата реакция в батерията ви позволява многократно да разреждате и зареждате батерията. Това е предимството на батериите пред източниците на ток за еднократна употреба, обикновените батерии, при които е възможен само ток за разреждане.
Като среда за прехвърляне на заряд от един електрод на акумулатора към друг се използва електролит - специално решение, поради химическата реакция на което с материала върху електродите са възможни както директни, така и обратни химически реакции в акумулатора, което прави възможно зареждането на батерията и неговото звание.
Днес един от най-обещаващите видове батерии е литиево-йонна батерия, В тези батерии алуминият действа като отрицателен електрод (катод), а медът като положителния електрод (анод). Електродите могат да имат различна форма, като правило това е фолио под формата на цилиндър или продълговата опаковка.
Нанесете върху алуминиево фолио катоден материал, който най-често може да бъде един от трите: литиев кобалтат LiCoO2, литиев ферофосфат LiFePO4 или литиев манганов шпинел LiMn2O4, а графитът се нанася върху медно фолио. Литиевият ферофосфат LiFePO4 е единственият понастоящем безопасен катоден материал по отношение на опасност от експлозия и екологичност.

Полимерните електролити, които могат да включват литиеви соли в състава си, поради своята пластичност позволяват да се произвеждат литиево-йонни батерии с голяма вътрешна повърхност и почти всяка форма, а това значително увеличава както производствеността на производството, така и общите размери.
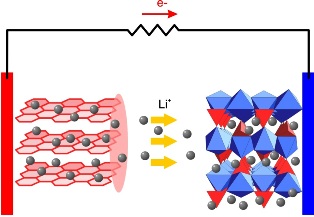
В процеса на зареждане на такава батерия литиевите йони се движат през електролита и се вграждат в кристалната решетка на графита върху анода, образувайки литиево-графитно съединение LiC6, По време на разряда възниква обратният процес - литиевите йони се придвижват към катода (окислител) от анода, а електроните се придвижват към катода във външната верига, в резултат на това процесът придобива електрическа неутралност.
Номиналното напрежение на литиево-йонна батерия е 3,6 волта, но потенциалната разлика по време на зареждане може да достигне 4,23 волта. Във връзка с този факт зарядът се произвежда при максимално допустимо напрежение не повече от 4,2 волта.
Някои литиеви съединения могат лесно да се запалят, ако напрежението е надвишено, поради което традиционно те са вградени в литиево-йонни батерии контролери за ниво на зарежданекоито не позволяват превишаване на критичното напрежение. Друга функция за безопасност е интегрираният клапан за облекчаване на излишното налягане вътре в чантата.
Литиево-йонните батерии вече са заели своето достойно място на пазара на преносими домакински уреди. Това са батерии за мобилни телефони, камери, видеокамери, таблети, плейъри и т.н.

Литиев ферофосфат LiFePO4 Счита се за най-обещаващия катоден материал поради неговата екологичност. Литиевият кобалтат LiCoO2 от своя страна е токсичен и вреден за околната среда, а за батерии, базирани на него, само 50% от йоните могат да бъдат отстранени от структурата на съединението, защото ако премахнете напълно лития от него, структурата ще стане нестабилна, кобалтът ще премине в състояние на окисляване + 4 и ще може да окисли кислорода и освободеният атомен кислород ще окисли електролита и ще възникне експлозия.Батериите с повишен капацитет (базирани на LiCoO2) са изключително експлозивни.
Литиевият ферофосфат LiFePO4 е предложен като катоден материал на батерии за по-мощни устройства през 1997 г. от Джон Гуденхоу.
Литиевият ферофосфат присъства в земната кора и няма да създаде никакви екологични проблеми в бъдеще. Кислородът не може да се освободи от него, тъй като всички те са силно свързани с фосфор с образуването на стабилен фосфатен йон. За възможността за използване на този материал обаче той трябваше да бъде фрагментиран на малки частици, в противен случай той ще остане изолатор поради много ниската си проводимост. Частиците бяха направени ламелни с малки размери по посока на движението на литиеви йони, след това покрити с въглероден слой с дебелина от нанометър.
Такива наночастици LiFePO4 са в състояние да се зареждат за 10 минути и ако покритието все още се модифицира, времето за зареждане ще бъде намалено до 1-3 минути. В бъдеще именно този материал ще може да осигурява мощност на електрическите превозни средства за 10 години. Вече технологично възможен цикъл на зареждане-заряд за 5-10 минути с пълна безопасност.
От гледна точка на съвременната наука, развитието и освобождаването на равномерното преносим наноакумулатор Няма да отнеме много време и думата е само за широкото технологично изпълнение на разработките. Що се отнася до перспективите на електрическите превозни средства, сега вече можем да предположим, че те ще станат основният вид транспорт в градовете в близко бъдеще.
Вижте също на e.imadeself.com
:

