Kategorijas: Piedāvātie raksti » Interesantas elektriskās ziņas
Skatījumu skaits: 15067
Komentāri par rakstu: 1
Litija jonu baterijas
 Jebkura elektriskā akumulatora darbības princips ir elektriskās enerģijas uzkrāšanās ķīmiskās reakcijas laikā, kas notiek, kad caur akumulatoru plūst uzlādēšanas elektriskā strāva, un elektriskās enerģijas ģenerēšana, kad izplūdes strāva plūst apgrieztas ķīmiskās reakcijas laikā.
Jebkura elektriskā akumulatora darbības princips ir elektriskās enerģijas uzkrāšanās ķīmiskās reakcijas laikā, kas notiek, kad caur akumulatoru plūst uzlādēšanas elektriskā strāva, un elektriskās enerģijas ģenerēšana, kad izplūdes strāva plūst apgrieztas ķīmiskās reakcijas laikā.
Baterijas ķīmiskās reakcijas atgriezeniskums ļauj atkārtoti izlādēt un uzlādēt akumulatoru. Šī ir bateriju priekšrocība salīdzinājumā ar vienreizējās lietošanas strāvas avotiem, parastajām baterijām, kurās ir iespējama tikai izlādes strāva.
Kā līdzeklis uzlādes pārnešanai no viena akumulatora elektrodu uz otru tiek izmantots elektrolīts - īpašs risinājums, kura ķīmiskās reakcijas dēļ ar materiālu uz elektrodiem akumulatorā ir iespējamas gan tiešas, gan apgrieztas ķīmiskas reakcijas, kas dod iespēju uzlādēt akumulatoru un viņa rangs.
Mūsdienās ir viens no daudzsološākajiem bateriju veidiem litija jonu akumulators. Šajās baterijās alumīnijs darbojas kā negatīvs elektrods (katods), bet varš - kā pozitīvs elektrods (anods). Elektrodiem var būt atšķirīga forma, parasti folija cilindra vai iegarenas paketes formā.
Uzklājiet uz alumīnija folijas katoda materiāls, kas visbiežāk var būt viens no trim: litija kobaltāts LiCoO2, litija ferofosfāts LiFePO4 vai litija mangāna spinelis LiMn2O4, un grafīts tiek uzklāts uz vara folijas. Litija ferofosfāts LiFePO4 ir vienīgais, šobrīd drošais katodu materiāls, ņemot vērā eksplozijas bīstamību un videi draudzīgumu kopumā.

Polimēru elektrolīti, kas savā sastāvā plastiskuma dēļ var iekļaut litija sāļus, ļauj ražot litija jonu akumulatorus ar lielu iekšējo virsmu un gandrīz jebkuru formu, un tas ievērojami palielina gan produkcijas izgatavojamību, gan vispārējos izmērus.
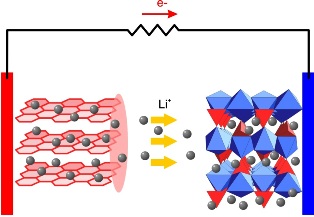
Šādas akumulatora uzlādes laikā litija joni pārvietojas caur elektrolītu un tiek iestrādāti anoda grafīta kristāla režģī, veidojot anodu litija grafīta savienojums LiC6. Izlādes laikā notiek apgrieztais process - litija joni no anoda pārvietojas uz katodu (oksidētāju), un elektroni pārvietojas ārējā ķēdē uz katodu, kā rezultātā process iegūst elektrisko neitralitāti.
Litija jonu akumulatora nominālais spriegums ir 3,6 volti, tomēr potenciālā starpība lādēšanas laikā var sasniegt 4,23 voltus. Saistībā ar šo faktu lādiņš tiek ražots ar maksimālo pieļaujamo spriegumu, kas nepārsniedz 4,2 voltus.
Daži litija savienojumi var viegli aizdegties, ja tiek pārsniegts spriegums, tāpēc tradicionāli tie tiek iebūvēti litija jonu akumulatoros uzlādes līmeņa kontrolierikas nepieļauj kritiskā sprieguma pārsniegšanu. Vēl viena drošības funkcija ir integrētais vārsts, kas mazina lieko spiedienu maisa iekšpusē.
Litija jonu akumulatori jau ir ieņēmuši savu likumīgo vietu pārnēsājamo sadzīves tehnikas tirgū. Tās ir baterijas mobilajiem tālruņiem, kamerām, videokamerām, planšetdatoriem, atskaņotājiem utt.

Litija ferofosfāts LiFePO4 Videi draudzīguma dēļ tas tiek uzskatīts par daudzsološāko katodu materiālu. Litija kobaltāts LiCoO2, savukārt, ir toksisks un videi kaitīgs, un akumulatoriem, kuru pamatā ir tikai 50% jonu, no savienojuma struktūras var tikt noņemti, jo, ja jūs pilnībā noņemsit litiju no tā, struktūra kļūs nestabila, kobalts nonāks oksidācijas stāvoklī + 4 un spēs oksidēt skābekli, un atbrīvotais atomu skābeklis oksidēs elektrolītu, un notiks eksplozija.Baterijas ar paaugstinātu ietilpību (pamatojoties uz LiCoO2) ir īpaši sprādzienbīstamas.
John Goodenough 1997. gadā ierosināja litija ferofosfātu LiFePO4 kā jaudīgāku ierīču bateriju katodu materiālu.
Litija ferofosfāts atrodas zemes garozā un nākotnē neradīs nekādas vides problēmas. No tā nevar atbrīvot skābekli, jo tas viss ir ļoti stingri saistīts ar fosforu, veidojot stabilu fosfāta jonu. Tomēr, lai izmantotu šo materiālu, tas bija jāsadala mazās daļiņās, pretējā gadījumā tā ļoti zemās vadītspējas dēļ paliks izolators. Daļiņas tika izgatavotas ar maziem izmēriem lamelārām pa litija jonu kustības virzienu, pēc tam pārklātas ar nanometru biezu oglekļa slāni.
Šādas LiFePO4 nanodaļiņas var uzlādēt 10 minūtēs, un, ja pārklājums joprojām tiek modificēts, tad uzlādes laiks tiks samazināts līdz 1-3 minūtēm. Nākotnē tieši šis materiāls 10 gadu laikā spēs nodrošināt enerģiju elektriskajiem transportlīdzekļiem. Jau tehnoloģiski iespējams uzlādes-izlādes cikls 5-10 minūtēs ar pilnīgu drošību.
No modernās zinātnes viedokļa, izlīdzināšanas attīstība un atbrīvošana pārnēsājams nanoakumulators Nebūs ilgi jāgaida, un vārds ir tikai attīstības plašajai tehnoloģiskajai ieviešanai. Runājot par elektrisko transportlīdzekļu izredzēm, tagad mēs jau varam pieņemt, ka tie tuvākajā nākotnē kļūs par galveno transporta veidu.
Skatīt arī vietnē e.imadeself.com
:

